一、医疗器械注册申请受理数据分析
据国家药监局网站数据,2021年共受理医疗器械首次注册、延续注册和变更注册申请12255项,与2020年相比增加15.8%。
1、按注册地域区分,受理境内第三类医疗器械注册申请5338项,受理进口医疗器械注册申请6917项。
2、按注册品种区分,医疗器械注册申请8540项,体外诊断试剂注册申请3715项。
3、按注册形式区分,首次注册申请2750项,占全部医疗器械注册申请的22.4%;延续注册申请5875项,占全部医疗器械注册申请的48%;变更注册申请3630项,占全部医疗器械注册申请的29.6%。
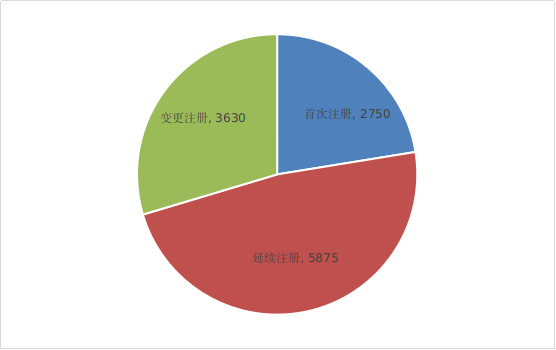
*注册形式比例图
二、医疗器械注册审批数据分析
2021年,国家药监局共批准医疗器械首次注册、延续注册和变更注册11314项,与2020年相比注册批准总数量增长14.9%。
其中,首次注册1710项,与2020年相比增加8.8%。延续注册6939项,与2020年相比增加25.6%。变更注册2665项,与2020年相比减少3.1%。
2021年,企业自行撤回注册申请182项,自行注销注册证书49项。
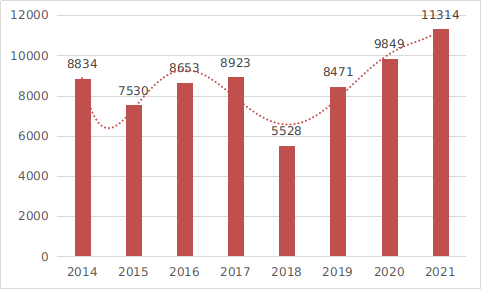
*2014至2021年度注册数据图
1、按照注册地域区分,境内第三类医疗器械注册4596项,与2020年相比增加27.6%,进口医疗器械6718项,与2020年相比增加7.6%。
2、按照注册品种区分,医疗器械7844项,占全部医疗器械注册数量的69.3%;体外诊断试剂3470项,占全部医疗器械注册数量的30.7%。
3、按照注册形式区分,首次注册1710项,占全部医疗器械注册数量的15.1%;延续注册6939项,占全部医疗器械注册数量的61.3%;变更注册2665项,占全部医疗器械注册数量的23.6%。
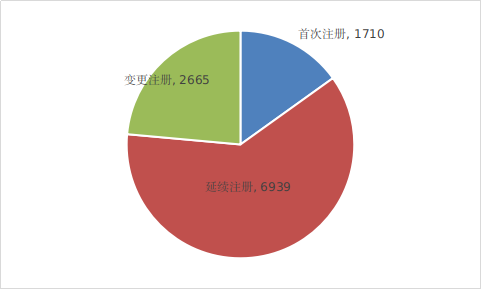
2021年注册形式比例图
三、进口医疗器械国别数据分析
2021年,共有27个国家(地区)产品在我国获批上市,其中,美国、德国、日本、韩国、瑞士医疗器械在中国医疗器械进口产品首次注册数量排前5位,注册产品数量约占2021年进口产品首次注册总数量的72.5%,与2020年基本持平。
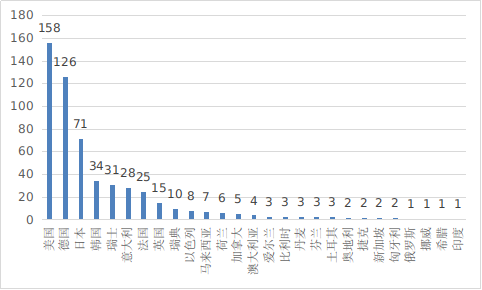
进口医疗器械注册国别排位图
从进口医疗器械代理人分布分析,共有13个省涉及有本省企业作为进口医疗器械代理人,其中上海市代理人代理的进口首次医疗器械数量最多,占全部进口医疗器械数量的60.1%。
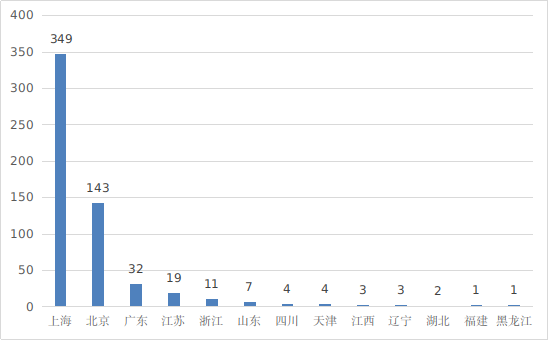
代理人代理的进口医疗器械数量省份排位图
四、境内第三类医疗器械省份分析
从2021年境内第三类医疗器械注册情况看,相关注册人主要集中在沿海经济较发达省份。其中,江苏、广东、北京、上海、山东是境内第三类医疗器械首次注册数量排前五名的省份,占2021年境内第三类医疗器械首次注册数量的67.9%,与2020年相比增加4.9%。
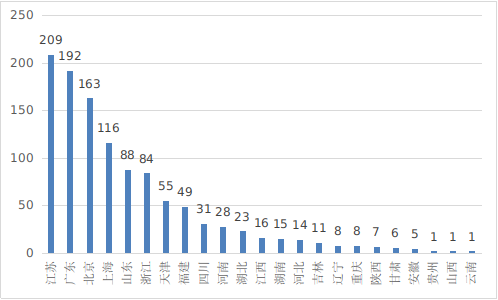
*境内第三类医疗器械注册省份排位图
五、创新医疗器械等产品注册数据分析
2021年,国家药监局按照《创新医疗器械特别审查程序》《医疗器械优先审批程序》继续做好相关产品的审查工作,共收到创新医疗器械特别审批申请249项,比2020年增加26.4%,其中62项获准进入特别审查程序,收到优先申请41项,比2020年增加46.3%,其中14项获准优先审批。
从2014年至2021年,国家药监局共批准134个创新医疗器械,其中,境内创新医疗器械涉及14个省的104家企业,进口创新医疗器械涉及2个国家的5个企业。
北京、上海、广东、江苏、浙江创新医疗器械获批产品数量和相应企业数量最多,约占全部已批准的134个创新医疗器械的81%。
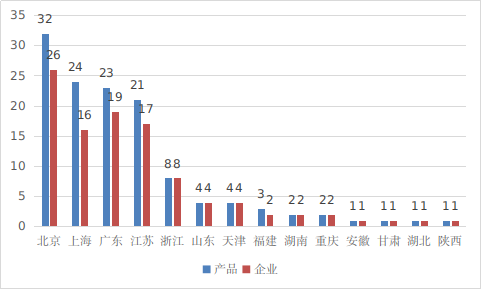
*境内创新医疗器械注册省份排位图
2021年,国家药监局共批准35个创新医疗器械产品上市,相比2020年,增加35%。这些创新产品核心技术都有我国的发明专利权或者发明专利申请已经国务院专利行政部门公开,产品主要工作原理/作用机理为国内首创,具有显著的临床应用价值。
六、其他注册管理情况
(一)境内第二类医疗器械注册审批数据分析
2021年,各省级药品监管部门共批准境内第二类医疗器械注册31509项,与2020年相比增加6.3%。其中,首次注册13041项,与2020年相比减少9.5%。首次注册项目占全部境内第二类医疗器械注册数量的41.4%。
延续注册11429项,与2020年相比增加24.5%,占全部境内第二类医疗器械注册数量的36.3%;变更注册7039项,与2020年相比增加16.1%,占全部境内第二类医疗器械注册数量的22.3%。
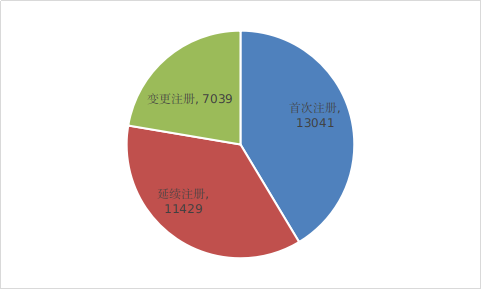
*境内第二类医疗器械注册形式比例图
(二)第一类医疗器械备案情况
2021年,国家药监局依职责共办理进口第一类医疗器械备案数量1854项,与2020年相比增加0.5%。
全国设区的市级药品监管部门依职责共办理境内第一类医疗器械备案数量26773项,与2020年相比减少22.7%。
(三)登记事项变更/变更备案情况
2021年,国家药监局依职责共办理进口第二、三类和境内第三类医疗器械登记事项变更/变更备案4603项,与2020年相比增加0.6%。
其中,境内第三类医疗器械登记事项变更/变更备案2455项,进口第二类、三类医疗器械登记事项变更/变更备案2148项。
各省级药品监管部门依职责共办理境内第二类医疗器械登记事项变更/变更备案10731项,与2020年相比增加31.4%。
(四)医疗器械临床试验机构备案情况
自2018年1月1日《医疗器械临床试验机构条件和备案管理办法》颁布实施以来,全国共计31个省、自治区、直辖市1074个机构完成了医疗器械临床试验机构备案工作。其中广东省、山东省、江苏省、北京市、上海市临床试验机构备案数量居全国前五名。
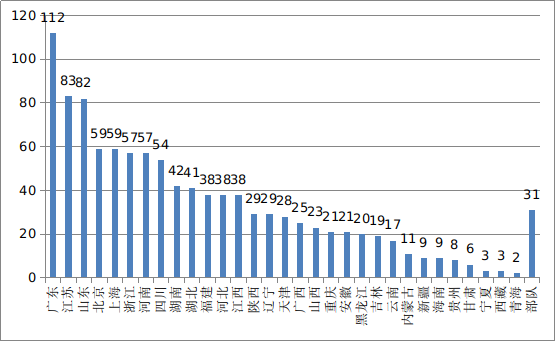
*全国医疗器械临床试验机构备案数量
注:本报告的数据源自国家药品监督管理局网站 智诚联帮整理